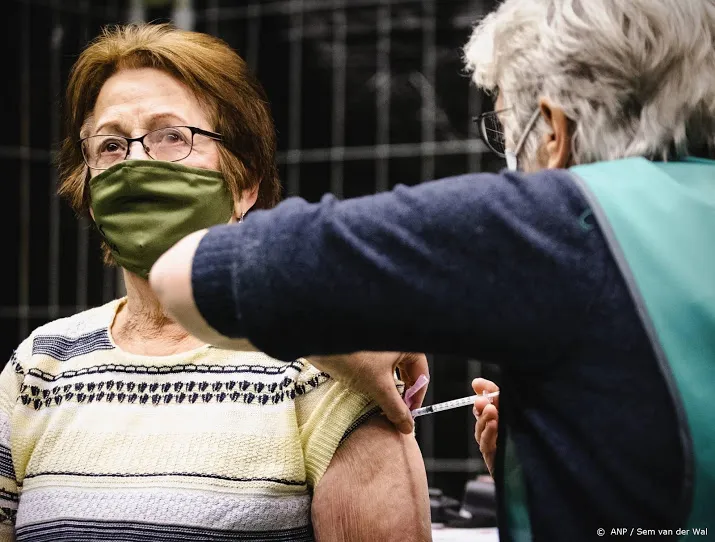
Leidse farmaceut Janssen vraagt om goedkeuring coronavaccin
Het farmaceutische bedrijf Janssen uit Leiden wil zijn coronavaccin op de markt brengen. Het heeft een voorwaardelijke toelating aangevraagd. Dat laat de Europese toezichthouder, het Europees Geneesmiddelenbureau (EMA) weten. Als dat bureau een positief oordeel geeft, is het aan de Europese Commissie om het middel toe te laten. Dat oordeel komt waarschijnlijk half maart, laat het EMA weten, en meestal volgt het besluit van de Commissie snel.
Nederland heeft 11,3 miljoen doses van het vaccin van Janssen besteld.
Het EMA keek de afgelopen tijd al mee met proeven met het coronavaccin. De beoordelaars kunnen dan sneller een oordeel vormen over de werking en de veiligheid van het middel. Dat wordt een rolling review genoemd.
Het vaccin uit Leiden bestaat uit een ander viruslichaam, een zogeheten adenovirus, waaraan de genetische code voor de uitsteeksels van het coronavirus is toegevoegd. Die code zorgt voor het eiwit waardoor het coronavirus een cel vastgrijpt en het lichaam binnendringt. Het vaccin zorgt ervoor dat cellen proberen dat eiwit aan te maken, waarna het afweersysteem probeert die indringer aan te vallen. Zo kan de afweer het virus bij een volgende besmetting herkennen en bestrijden, is de gedachte. "Het adenovirus in het vaccin kan zich niet vermenigvuldigen en maakt mensen niet ziek", benadrukt het EMA.
Tot nu toe zijn drie coronavaccins in de Europese Unie op de markt gebracht. Het zijn de middelen van Pfizer/BioNTech, Moderna en AstraZeneca. Daarnaast kijken de inspecteurs alvast mee bij de kandidaatvaccins van Novavax en CureVac.